JBO竞博Insight 数据库全球新药模块重磅升级!
JBO竞博囊括全球近4万个新药、改良新及类似药项目,将临床前到获批上市全流程打通,每日持续更新,信息准确可溯源,并提供多样化的筛选及分析功能,让企业决策更精准,工作更高效。


本文将以ADC领域新药开发为例,选取部分功能使用场景做简单介绍。Insight 数据库同时还拥有医药交易和临床试验结果功能,后续将陆续公开获取及使用指南,敬请期待!
* 以下数据截至2022年6月28日,更多信息欢迎使用Insight数据库查询
据丁香园 Insight 数据库全球新药模块显示,当前全球已有587个ADC新药在开发。通过「可视化」浏览全局情况,全球共15个ADC药物获批上市,其中5个已在中国获批;临床试验阶段新药更是项目众多,全球有281个已启动临床的ADC药物,71个在中国已进入临床开发阶段。

Insight 数据库全球新药模块提供丰富的境内外数据对比能力,可从全球、中国内地、境外3个不同维度,从临床I/II/III期到上市4个不同阶段分别对比展现新药开发趋势,还可通过境内外项目数量的对比一览全球概况。
从近7年趋势来看,全球ADC药物研发总体呈现稳中有升的态势,每年平均推动约20个新药进入I期临床,约5个新药进入III期研发当中,总体临床进展在2021年呈现小高峰。

将境内外I期临床项目趋势作对比,相较于境外项目新增量的下滑,国内的新项目增长势头无疑是十分显著的。

具体到各阶段项目总数对比,可以看到国内处于III期研发的ADC项目数高于境外,正在进入爆发期,未来几年有望迎来多款新药报批。

点击图表中相应数据点,可跳转至原始数据列表,查看每一个项目的详情信息。如2021年度在中国进入I期临床的ADC新药共有16个,恒瑞医药独占4个,遥遥领先。

其中,华东医药的FRα ADC进展最快,该药为2020年10月引进自ImmunoGe公司的品种,2019年中国已经参与到其国际多中心III期临床试验中,华东医药引进后又于2021年启动了一项I期临床,2022年初登记了一项针对中国人群的III期临床,离国内申报上市已经不远。

若要分析国内企业参与的ADC项目,Insight 数据库中[企业总部所在国家]选项可以实现。选择总部位于中国的企业,可以看到目前这些ADC新药在境外开展的临床试验还比较少,国产创新药出海空间仍旧很大。

检索ADC药物,通过企业排名详情,可以看到同领域重点布局企业。组合使用Insight 数据库的丰富筛选项,可辅助对更细分赛道做分析。
全球来看,ADC龙头当属Seagen,该公司拥有44个ADC新药。而把目标锁定在国内,从项目数来讲,TOP5企业分别为多禧生物(18)、荣昌生物(12)、普方生物(11)、百利天恒药业(11)、恒瑞医药(9)、美雅珂(9)。

光标移至相应柱子,可以看到目标企业项目所处阶段概况,点击柱子即可跳转至项目清单,一览各项目靶点适应症等详细信息。多禧生物是ADC领域榜首,拥有18个ADC项目。虽然大多处于临床前,但潜力无限。普方生物与多禧生物同样,当前项目均为临床前。

荣昌生物则是国内进展最快的企业,首款ADC新药已经上市成为国产首款,3个品种也已经进入临床。而论起临床阶段ADC项目最多的企业则当属恒瑞,该公司有8个已经进入临床研究的ADC药物,其中3个在境外也开展了临床试验。

具体分析荣昌生物的管线详情,筛选「新药类型」为新药或该良新,可一览目前荣昌生物在研产品。切换至「按可视化」即可得到相关的可视化图表,结果更加一目了然。
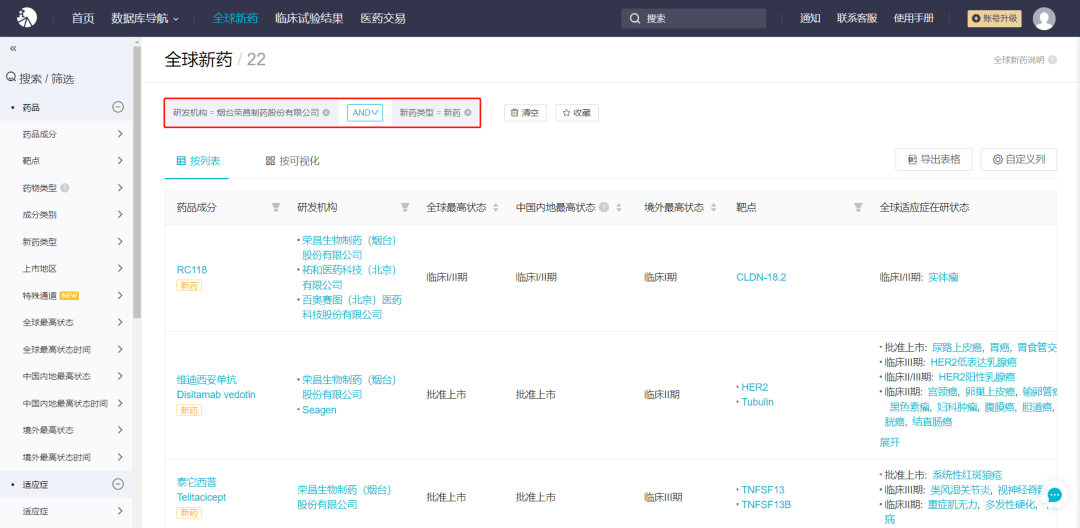
当前,荣昌生物共有22款新药在研,其中已获批上市的2款,而处于早期阶段的产品共有16款(含临床前以及临床 I 期阶段)。点击甘特图,即可跳转到相应的品种列表进而查看详细信息,如获批上市的两款产品分别为维迪西妥单抗和泰它西普JBO竞博。

从成分类别来看,荣昌生物在研新药以ADC为主,共有12款,占比约为55%,此外,还布局了双抗、单抗等。

从适应症来看,荣昌生物研发管线覆盖自身免疫、抗肿瘤、眼科等领域,其中以肿瘤领域为主。
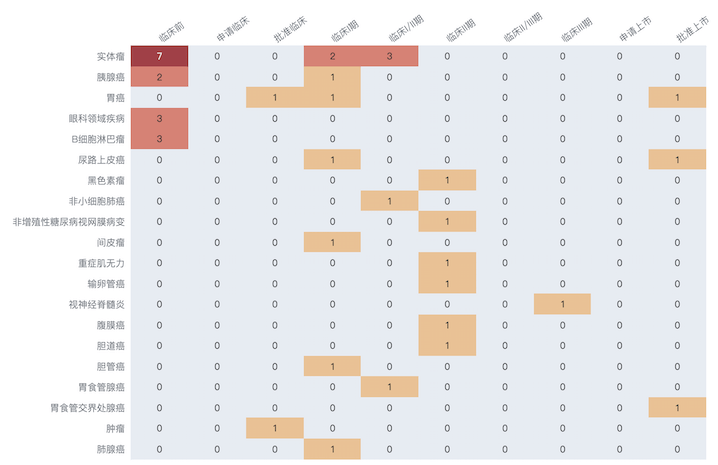
而从靶点布局情况来看,除HER2外,还重点布局了CD19(3 款)和EGFR(2 款)。

在项目详情页,可查看重点项目全球开发情况,如重点项目开发重要节点、适应症全球开发进展、临床试验登记及结果、重要医药交易事件等全生命流程信息。下面以荣昌生物的核心产品「维迪西妥单抗」为例。
打开项目详情,首先可以看到新药的简介、结构/机制、靶点、成分类别、研发机构等基本信息。在药品名称下方,可以看到该药在全球各国的优先审评通道、突破性疗法和附条件批准纳入情况。

「项目概览」板块清晰展示了该项目的重点事件及时间节点。维迪西妥单抗于2015年9月在国内获批临床,同年12月首次启动临床,2020年8月首次申报上市,去年6月首次获批上市。而在境外,维迪西妥单抗于2021年4月在美国时首次公示临床。

在「获批适应症」板块中,可看到维迪西妥单抗已获批上市的适应症、用药方案、获批时间、国家/地区、疗法类型以及用药人群。原始适应症均提供溯源,可一键直达官方信源。
可以看到,在2021年6月维迪西妥单抗首次获批用于至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)患者的治疗。此后于今年1月再次获批,用于治疗既往接受过系统化疗且HER2阳性( HER2阳性为免疫组化检查结果为2+或3+)的局部晚期或转移性尿路上皮癌(UC)患者。
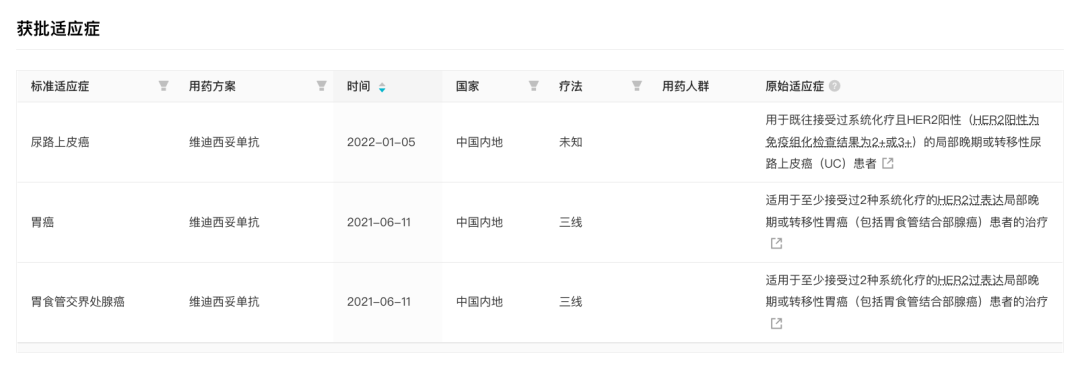
当前,维迪西妥单抗在全球已登记有22项临床试验。除胃癌、尿路上皮癌外,还在开展多项针对乳腺癌、胆道癌、结直肠癌等10余个癌种的临床研究。除中国外,还在美国也登记开展了临床试验。
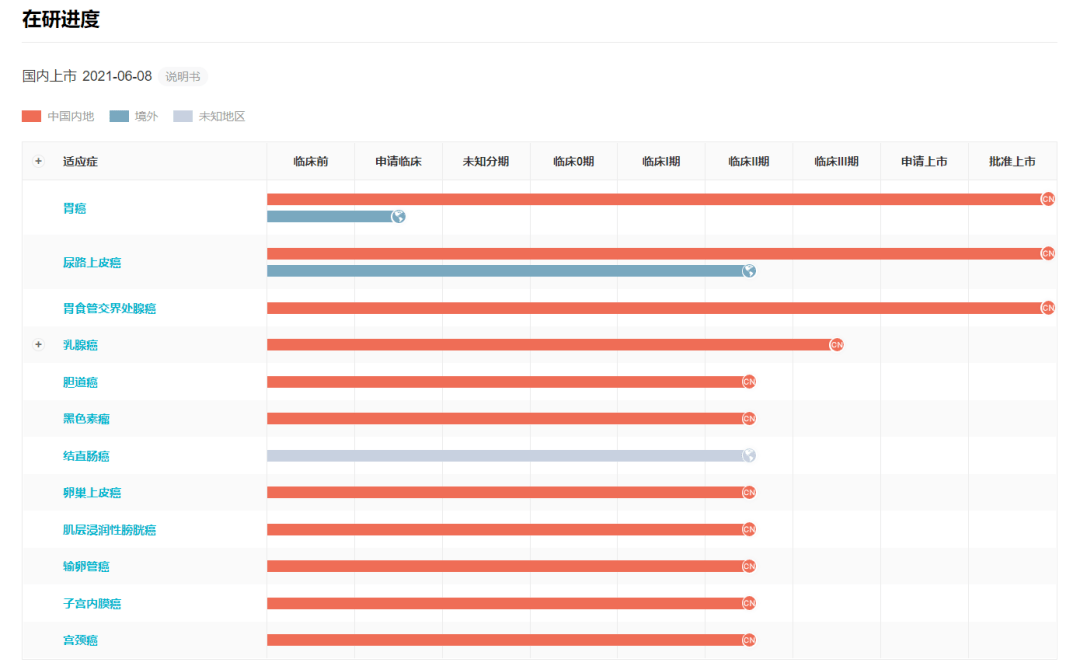
在「甘特图」中,可以根据检索需求筛选查看目标新药的特定适应症在特定地区不同研发阶段的相应进度。
如查看除已获批适应症之外进展最快的乳腺癌适应症,维迪西妥单抗目前正在开展一项随机、对照、多中心III期临床研究,旨在评价该药治疗HER2低表达局部晚期或转移性乳腺癌有效性和安全性。2020年9月该研究已经在国内完成首例患者的入组工作。
如筛选[乳腺癌]适应症,目前维迪西妥单抗已有3项临床试验结果分别在2018 ASCO和2021 ASCO中公布,均为I期C003 CANCER试验结果。其中既包括治疗HER2阳性乳腺癌的初步数据,也包括针对HER2低表达乳腺癌的I期临床试验数据。

在出海进展方面,2021年8月9日,荣昌生物以2亿美元首付款+最高24亿美元里程碑付款将维迪西妥单抗授权给海外ADC巨头Seagen,该公司保留在包括大中华区、亚洲所有其他国家(日本、新加坡除外)开发和商业化维迪西妥单抗的权益,而Seagen将获得以上许可地区之外的全球开发和商业化权益。

文章篇幅有限,只展示了部分功能,更多新功能可以点击文末「阅读原文」申请免费试用~返回搜狐,查看更多

